
企業(yè)新聞 品牌專欄 案例報(bào)道 企業(yè)文化 技術(shù)文章 產(chǎn)品評(píng)測(cè)
2016年09月12日 09:06上海恒遠(yuǎn)生物科技有限公司點(diǎn)擊量:3485
CD47抗體幾乎一夜爆紅,大家不禁思考CD47 mAbs會(huì)是下一個(gè)PD1/PD-L1嗎?讓我們一起來(lái)了解下CD47抗體到底是什么。
CD47是什么?
CD47也被稱為整合素相關(guān)蛋白(integrin associated protein,IAP),是免疫球蛋白超家族成員。CD47廣泛的表達(dá)于細(xì)胞的表面,可與信號(hào)調(diào)節(jié)蛋白α (Signal regulatory protein α , SIRP α)、血小板反應(yīng)蛋白(thrombospondin-1, TSP1)以及整合素(integrins)相互作用,介導(dǎo)凋亡、增殖、免疫等一系列的反應(yīng)[1,2]。
CD47是"自我"信號(hào),代表"別吃我"
人體需要20-30 trillion的紅細(xì)胞,以此保持氧氣有效的運(yùn)輸?shù)饺砀魈帯<t細(xì)胞的生命周期較短僅有120天,每小時(shí)有100億的紅細(xì)胞生成,也有無(wú)數(shù)衰老的紅細(xì)胞被巨噬細(xì)胞吞噬清除(Fig1)。
然而巨噬細(xì)胞是如何區(qū)分年輕和衰老的紅細(xì)胞,只進(jìn)攻衰老紅細(xì)胞的機(jī)理卻不為人知。
直到2000年,Oldenborg等人證實(shí)CD47是細(xì)胞表面一個(gè)重要的"self"標(biāo)記,是調(diào)節(jié)巨噬細(xì)胞吞噬作用的一個(gè)重要信號(hào)。CD47可以與巨噬細(xì)胞表面SIRPα結(jié)合,磷酸化其ITIM,隨后招募SHP-1蛋白,產(chǎn)生一系列的級(jí)聯(lián)反應(yīng)抑制巨噬細(xì)胞的吞噬作用。(Fig2)
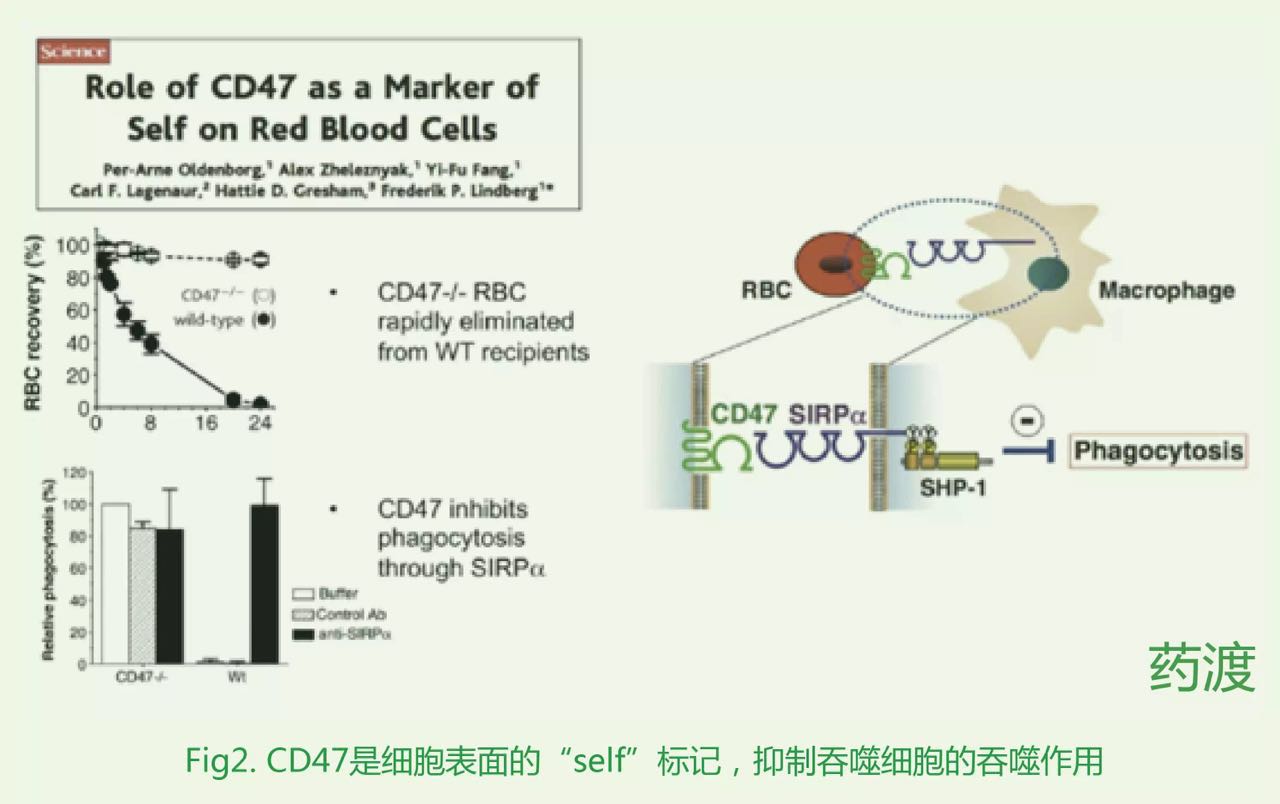
年輕的紅細(xì)胞表達(dá)較高的CD47向巨噬細(xì)胞釋放"自己人,別吃我"的信號(hào),而衰老的紅細(xì)胞CD47下調(diào),zui終被巨噬細(xì)胞所清除[3]。
狡猾的腫瘤細(xì)胞高表達(dá)CD47躲避吞噬
腫瘤細(xì)胞有一系列躲避人體免疫系統(tǒng)追殺的方案,包括分泌免疫抑制因子、下調(diào)MHC I表達(dá),以及上調(diào)PD-L1抑制CD8+T細(xì)胞活性。
聰明的腫瘤細(xì)胞當(dāng)然不會(huì)放過(guò)CD47這個(gè)的掩體。不同的研究表明,幾乎所有的腫瘤細(xì)胞和組織都高表達(dá)CD47,是對(duì)應(yīng)正常細(xì)胞和組織的3倍。(Fig3)
通過(guò)CD47這個(gè)"self"信號(hào),腫瘤細(xì)胞有效的躲避了巨噬細(xì)胞的吞噬作用[4-6]。

CD47抗體的機(jī)理
機(jī)理一:
腫瘤細(xì)胞上調(diào)CD47的表達(dá),以此欺騙巨噬細(xì)胞。那么通過(guò)CD47抗體block這個(gè)"別吃我"的信號(hào),使巨噬細(xì)胞發(fā)揮吞噬作用,是一個(gè)非常容易理解的事情。(Fig4)
關(guān)于這個(gè)機(jī)理Forty Seven的創(chuàng)始人斯坦福大學(xué)的Weissman博士做了一系列的工作論證。
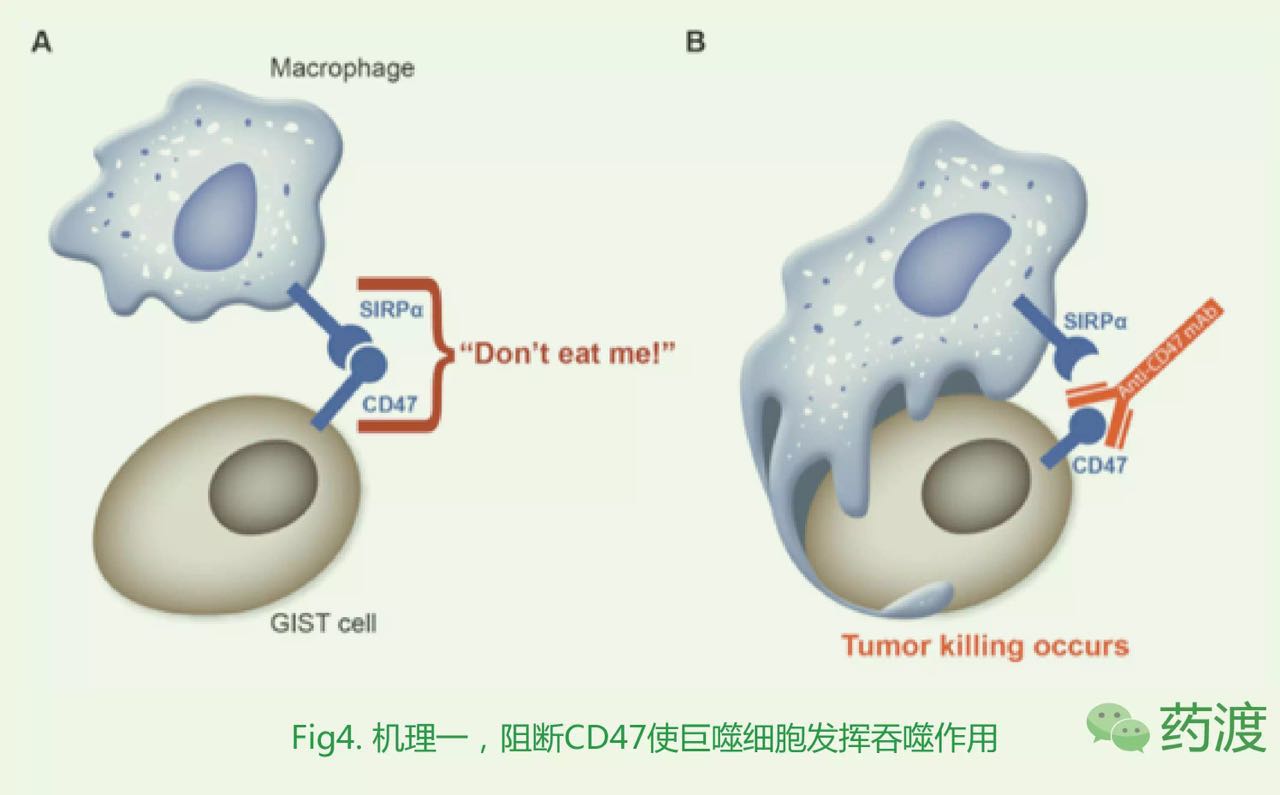
機(jī)理二:
Liu等人研究表明,CD47抗體治療是通過(guò)DC細(xì)胞和CD8+T發(fā)揮腫瘤殺傷效應(yīng)的。DC細(xì)胞通過(guò)CD47抗體和親吞噬分子協(xié)同作用,吞噬腫瘤細(xì)胞,并提呈腫瘤相關(guān)抗原給CD8+T,進(jìn)而發(fā)揮CD8+T對(duì)腫瘤的特異性殺傷作用[7]。(Fig5)
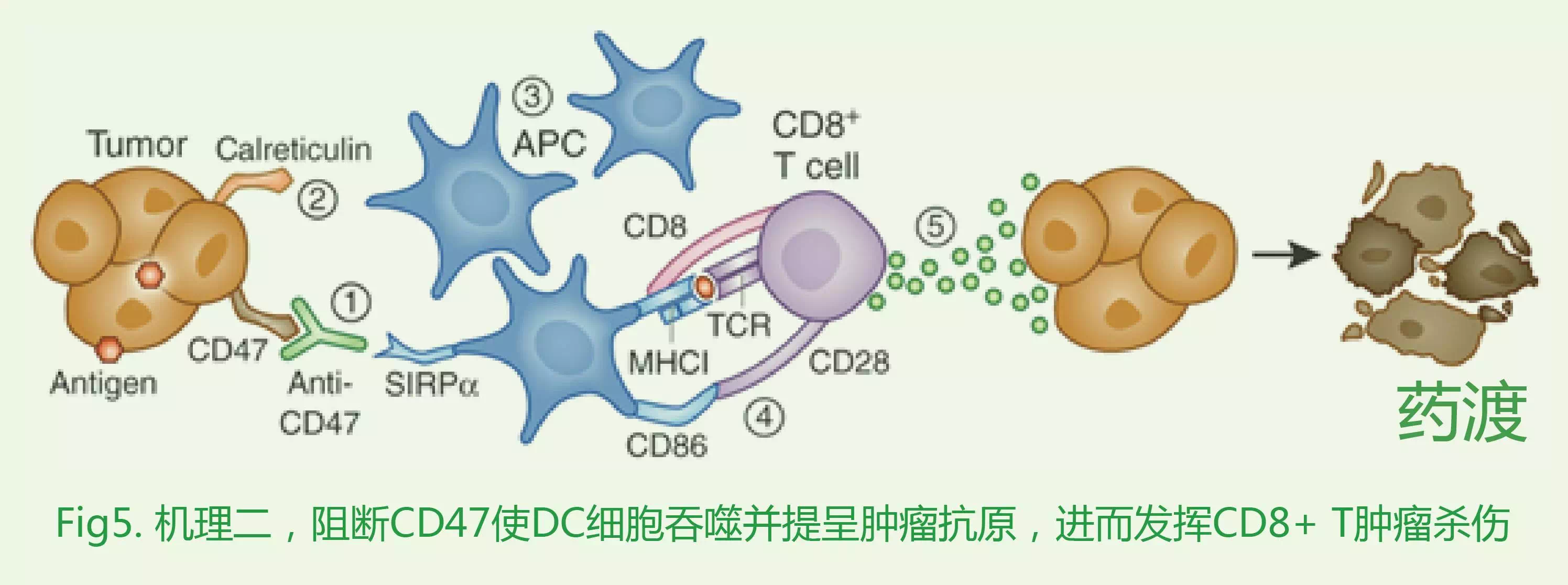
結(jié)合這兩個(gè)機(jī)理表明CD47抗體極有可能具有同時(shí)激活天然免疫以及適應(yīng)性免疫的能力。
CD47是一個(gè)理想的腫瘤治療靶點(diǎn)嗎?
拋開(kāi)有效性先不談,先看看安全性:
巨噬細(xì)胞發(fā)揮吞噬作用,不僅需要block CD47的"自己人,別吃我"信號(hào),也需要鈣網(wǎng)織蛋白(calreticulin,CRT)等“吃我”信號(hào)的協(xié)同作用。通常情況下腫瘤細(xì)胞高表達(dá)CRT而正常細(xì)胞并不表達(dá)CRT等"吃我"信號(hào),所以盡管CD47也廣泛在人的大腦皮層以及小腦等健康組織中,CD47抗體治療在正常組織中被認(rèn)為是沉默的。然而,觀察Phase 1的臨床數(shù)據(jù),接受放療和化療后的患者會(huì)上調(diào)"吃我"信號(hào)。CD47抗體治療后,CD47+紅細(xì)胞枯竭,造成短暫性的貧血是其主要的不良反應(yīng)。雖然該不良反應(yīng)在臨床上比較好控制,但是CD47抗體治療是否真的對(duì)正常組織沒(méi)有傷害,是目前zui為重要的一個(gè)問(wèn)題[8]。
有效性問(wèn)題:
動(dòng)物試驗(yàn)中,CD47抗體對(duì)于多種腫瘤治療皆具有顯著的效果[5,8]。目前CD47抗體的人體臨床試驗(yàn)皆在Phase 1階段,談?wù)撝委熜Ч€為時(shí)過(guò)早。CD47抗體能否到達(dá)腫瘤微環(huán)境中發(fā)揮作用,目前也未可知。
許多人都將CD47抗體看成PD1/PD-L1抗體之后,下一代腫瘤免疫抑制劑產(chǎn)品。
兩者確實(shí)有相似之處,CD47與PD-L1都受轉(zhuǎn)錄因子myc的調(diào)控[9];CD47與PD1/PD-L1都是負(fù)負(fù)得正的作用機(jī)制。
筆者認(rèn)為從某些方面來(lái)講,CD47抗體比PD1/PD-L1抗體更加具有吸引力。
首先是CD47具有更為廣泛的表達(dá),以及在所有腫瘤細(xì)胞中幾乎都高表達(dá),代表著其具有更為廣譜的效應(yīng).
第二,Liu等人工作表明,CD47抗體可以介導(dǎo)CD8+T對(duì)腫瘤的特異性殺傷作用[7]。PD-1、CTLA-4等腫瘤免疫抑制劑之所以僅對(duì)一小部分發(fā)揮作用,也許一個(gè)重要的原因就是PD-1/CTLA-4抗體,無(wú)法形成腫瘤特異性的T細(xì)胞priming[10]。
CD47抗體目前的研發(fā)格局
CD47抗體項(xiàng)目都處在早期,產(chǎn)品競(jìng)爭(zhēng)也沒(méi)有那么激烈。
根據(jù)BioCentury數(shù)據(jù)顯示,共有3個(gè)CD47抗體項(xiàng)目處于Phase 1階段、1個(gè)處于IND階段,以及4個(gè)臨床前階段。(Fig6)
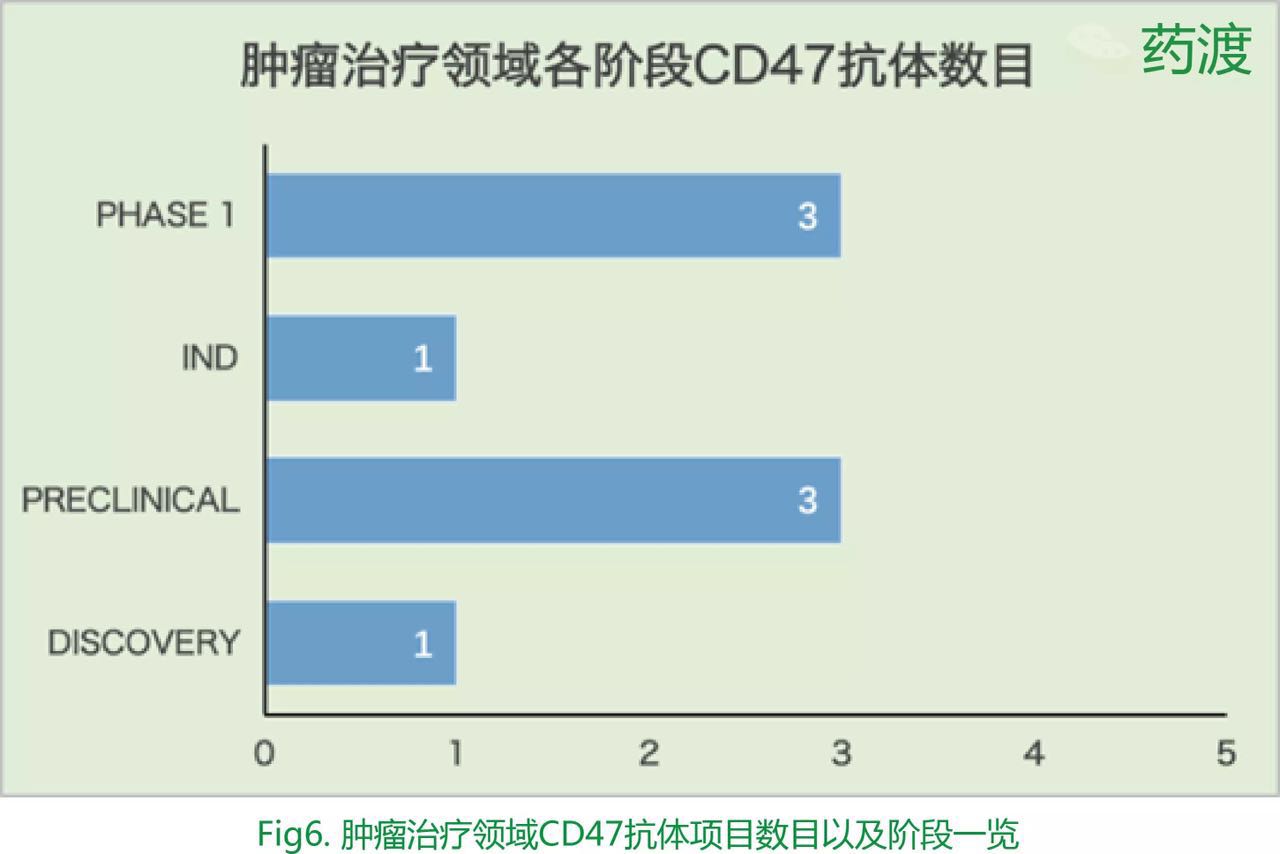
目前處于Phase 1的三個(gè)藥物分別為Forty Seven的Hu5F9-G4、Celgene的CC-90002(來(lái)自Inhibrx,原代碼為INBRX-103)以及Trillium的TTI-621。1期臨床數(shù)據(jù)會(huì)在2016年年底以及2017年陸續(xù)揭曉。
值得一提的是,Trillium Therapeutics的CD47抗體項(xiàng)目為SIRPαFc融合蛋白,與Hu5F9-G4具有相類似的CD47親和力(nM級(jí)別)。而SIRPαFc具有兩大優(yōu)勢(shì): 首先是其分子量更小約80kDa,相對(duì)于抗體分子的150kDa具有更好的穿透性和組織分布性;其次SIRPαFc對(duì)于紅細(xì)胞的親和力要遠(yuǎn)遠(yuǎn)低于Hu5F9-G4,表明其可能具有更好的安全性。
在CD47抗體的腫瘤治療領(lǐng)域,Trillium Therapeutics的SIRPαFc融合蛋白也許會(huì)有差異化的優(yōu)勢(shì)。
另外,進(jìn)展較快的還有novimmune的NI-1701,計(jì)劃于2017年的上半年開(kāi)展Phase 1臨床試驗(yàn)。
NI-1701是CD19與CD47的雙特異性抗體,通過(guò)CD19靶向腫瘤細(xì)胞,并阻斷CD47的"別吃我"信號(hào),同時(shí)利用Fc片段招募巨噬和NK等細(xì)胞發(fā)揮腫瘤殺傷作用。
CD19增加了NI-1701的特異性,保證了其安全性,但是相對(duì)來(lái)說(shuō)也影響了其作用的廣譜性。NI-1701很難應(yīng)用至B淋巴細(xì)胞腫瘤以外的腫瘤治療中。
本網(wǎng)轉(zhuǎn)載并注明自其它來(lái)源(非智慧城市網(wǎng)www.mms47.com)的作品,目的在于傳遞更多信息,并不代表本網(wǎng)贊同其觀點(diǎn)或和對(duì)其真實(shí)性負(fù)責(zé),不承擔(dān)此類作品侵權(quán)行為的直接責(zé)任及連帶責(zé)任。其他媒體、網(wǎng)站或個(gè)人從本網(wǎng)轉(zhuǎn)載時(shí),必須保留本網(wǎng)注明的作品第一來(lái)源,并自負(fù)版權(quán)等法律責(zé)任。
免費(fèi)注冊(cè)后,你可以
了解安防行業(yè)更多資訊查看安防行業(yè)供求信息凸顯安防行業(yè)自身價(jià)值 馬上注冊(cè)會(huì)員想快速被買家找到嗎
只需要發(fā)布一條商機(jī),被買家找到的機(jī)會(huì)高達(dá)90%!還等什么? 馬上發(fā)布信息
2025深圳國(guó)際智能安防展覽會(huì)-ISE安博會(huì)
2025深圳國(guó)際智能安防展覽會(huì)簡(jiǎn)稱“ISE安博會(huì)”。伴隨著智能【詳細(xì)】